乳腺癌是目前发病率最高的恶性肿瘤,也是全球女性癌症相关死亡的主要原因。尽管乳腺癌的治疗取得了长足的进展,但仍有大量患者因疾病复发和转移而死亡。乳腺癌肿瘤干细胞(BCSC)被定义为具有肿瘤起始特性和无限自我更新/增殖潜力的细胞,对肿瘤转移和复发至关重要。缺氧微环境在乳腺癌中普遍存在,而BCSC通常位于肿瘤内缺氧区域。因此,了解缺氧微环境对BCSC表型维持背后的分子机制对于开发更成功的治疗策略和提高乳腺癌患者的总体生存率至关重要。
近日,我院乳腺外科为第一完成单位及末尾通讯单位的原创性研究(Original Article)“HIF-1-regulated expression of calreticulin promotes breast tumorigenesis and progression through Wnt/β-catenin pathway activation”在《Proceedings of the National Academy of Sciences of the United States of America》杂志(缩写:PNAS,IF:11.205)上在线发表。该杂志为美国国家科学院的院刊,亦是世界四大百年经典期刊之一。
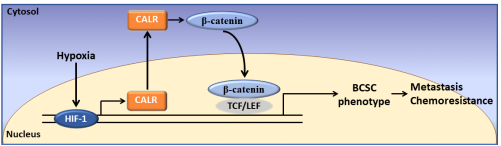
该研究发现钙网蛋白(CALR)在乳腺癌中高表达,且与患者的预后相关;并且首次报道了CALR是HIF-1的靶基因,HIF-1可以通过直接调控CALR基因的转录从而促进乳腺癌干细胞的表型维持,进而导致乳腺癌的发生、化疗耐药、侵袭和转移;深入的分子水平探索证实CALR通过WNT/β-catenin信号通路发挥以上生物学功能。以上关于CALR的创新性发现填补了HIF-依赖/缺氧诱导的WNT/β-catenin信号通路的活化与BCSC表型维持之间缺失的一环,为临床使用HIF-1和/或CALR的靶向药物治疗提供了新的理论支持。
该项工作是乳腺外科何建军教授团队和美国约翰霍普金斯大学医学院Gregg L. Semenza教授合作、在转化医学中心刘培军教授团队的技术和平台支持下完成,西安交通大学第一附属医院乳腺外科刘晓旭博士是该论文的第一作者,Gregg L. Semenza教授、何建军教授以及张慧敏医生为该论文的共同通讯作者。Gregg L. Semenza教授系2019年诺贝尔生理学或医学奖获得者、美国科学院院士、美国医学院院士、美国艺术与科学院院士,自2014年以来,何建军教授团队与Gregg L. Semenza教授建立长期合作关系,先后联合培养两名博士研究生,在《PNAS》发表系列研究成果3篇(PMID: 26512116;PMID: 33952697;PMID: 34706936)。乳腺外科何建军教授团队一直关注肿瘤微环境与肿瘤干细胞领域的基础研究、并致力于乳腺难治性疾病的转化和临床研究,通过持续的人才培养、交流合作,不断加强科研能力建设,旨在通过临床-转化-基础研究解决实际问题,改善乳腺疾病患者的预后。
文章链接:https://www.pnas.org/content/118/44/e2109144118