近日,我院生物样本信息资源中心王亚文、李晓娇团队在国际期刊《Journal of Controlled Release》(中科院一区,TOP期刊,影响因子11.5)上发表题为《Posttranslational remodeling micelle reverses cell-surface and exosomal PD-L1 immunosuppression in tumors resistant to PD-L1 antibody therapy》的研究论文。

免疫检查点阻断疗法在肿瘤治疗领域取得了革命性进展,然而肿瘤微环境(TME)中PD-L1的动态调控机制导致相当比例患者对PD-L1抗体治疗产生耐药。研究表明,这种耐药性与肿瘤细胞表面持续的PD-L1补充和PD-L1+的外泌体释放密切相关。针对这一关键科学问题,研究者开发了一种基于肿瘤微环境响应的纳米递药系统,通过共递送棕榈酰化抑制剂2-溴棕榈酸(2-BP)和化疗药物顺铂(DDP),实现了对PD-L1抗体耐药性黑色素瘤的有效治疗。
该研究首次系统阐明了2-BP通过抑制PD-L1棕榈酰化,同时阻断其细胞膜定位和外泌体分泌的双重作用机制。实验证实,2-BP可同时清除细胞表面及外泌体PD-L1,阻断肿瘤微环境与肿瘤引流淋巴结中的免疫抑制,而顺铂通过诱导免疫原性细胞死亡(ICD)促进T细胞浸润,与2-BP形成协同效应。此外,基于透明质酸(HA)和罗丹明110(Rho 110)的智能纳米载体可响应肿瘤微环境高浓度谷胱甘肽(GSH),实现药物的精准释放,减少全身毒性。
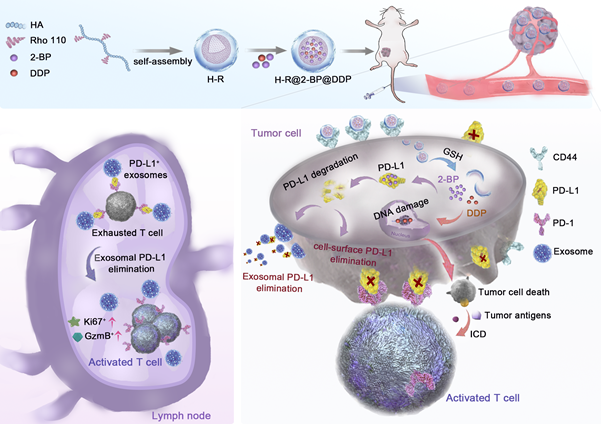
研究团队在PD-L1抗体耐药性黑色素瘤模型中验证了该策略的高效性,结果显示联合疗法不仅能显著抑制原发瘤生长、降低术后复发率和远处转移,还能诱导长效T细胞记忆,防止肿瘤再次攻击。该研究为PD-L1抗体低响应性肿瘤(如晚期黑色素瘤)提供了新治疗范式,其机制创新性在于首次通过靶向棕榈酰化实现PD-L1在细胞膜和外泌体上的双重耗竭,同时为化疗与免疫治疗的协同应用提供了理论依据。未来,团队计划进一步优化纳米载体配方,并探索其他PD-L1翻译后修饰的干预潜力,以扩大适应症范围。
本研究受国家自然科学基金、西安交通大学基本科研业务费支持。西安交通大学第一附属医院生物样本信息资源中心师雪和西安交通大学博士生赵谢君为该文章的共同第一作者,西安交通大学第一附属医院王亚文教授、西北工业大学戴亮亮教授、西安交通大学第一附属医院李晓娇副研究员为共同通讯作者。西安交通大学第一附属医院为第一单位。
